Главная страница
 Базы данных
Базы данных
 База данных свойств веществ (поиск)
База данных свойств веществ (поиск)
Свойства вещества:
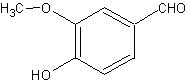
4-гидрокси-3-метоксибензальдегид
Синонимы и иностранные названия:
3-метокси-4-оксибензальдегид (рус.)
4-hydroxy-3-methoxybenzaldehyde (англ.)
vanillin (англ.)
ванилин (рус.)
Тип вещества:
органическое
Внешний вид:
бесцветн. моноклинные кристаллыБрутто-формула (по системе Хилла для органических веществ):
C8H8O3Формула в виде текста:
CH3O(HO)C6H3CHOМолекулярная масса (в а.е.м.): 152,147
Температура плавления (в °C):
82Температура кипения (в °C):
285Растворимость (в г/100 г растворителя или характеристика):
бензол: растворим (80°C) [Лит.]
вода: 1 (14°C) [Лит.]
вода: 5 (80°C) [Лит.]
глицерин: растворим [Лит.]
глицерин 25%: 2,36 (20°C) [Лит.]
глицерин 50%: 3,98 (20°C) [Лит.]
диэтиловый эфир: легко растворим [Лит.]
лигроин: растворим [Лит.]
пиридин: 316 (20°C) [Лит.]
пропиленгликоль: растворим [Лит.]
серная кислота: растворим [Лит.]
сероуглерод: растворим [Лит.]
уксусная кислота: растворим [Лит.]
хинолин: 5,51 (20°C) [Лит.]
хлороформ: легко растворим [Лит.]
этанол абсолютный: 67,22 (20°C) [Лит.]
Плотность:
1,056 (20°C, относительно воды при 4°C, состояние вещества - кристаллы)
Метод получения 1:
Источник информации: Патент Германии DE105,798 (от 15.09.1899)15 кг нитробензола нагревают с 45 кг дымящей серной кислоты до 120-130 С, до тех пор пока при пробе с водой не будет выделятся нитробензол. Сернокислотную смесь вносят затем в 600 л воды и охлаждают примерно до 15 С. К этому раствору прибавляют 10 кг гваякола и 8 кг 38%-ного формальдегида. При хорошем перемешивании вносят также постепенно 25 кг чугунных стружек. После стояния раствора в течение 24 часов отфильтровывают липкое бензилиденовое соединение, а раствор насыщают поваренной солью и отделяют ванилин и гваякол из фильтрата экстракцией эфиром. Отфильтрованное бензилиденовое соединение растворяют в растворе ацетата натрия и эфиром из этого раствора извлекают еще ванилин. Как и в предыдущем примере встряхивают эфирные вытяжки с раствором бисульфита и затем получают ванилин в свободном виде подкислением раствора. Ванилин кристаллизуется при охлаждении из кипящего лигроина в виде белых игл с температурой плавления 80 С.
Метод получения 2:
Источник информации: Патент Германии DE207,702 (от 10.03.1909)90 частей ацетилизоэвгенола окисляют с или без растворитения в 2800 частях воды с добавлением 20-30 частей сульфаниловой кислоты посредством смеси 280 частей дихромата калия и 300 частей серной кислоты. После завершения окисления извлекают получившийся ацетилванилин из реакционной смеси и затем изолируют в виде бисульфитного производного. После разложения и гидролиза получают чистый ванилин с хорошим выходом. Так получают 57 частей ванилина содержащего только 6,3 части непрореагировавшего ацетилизоэвгенола. Обработка без добавления сульфаниловой кислоты при равных условиях и пропорциях дает только 24,5 части ванилина, в котором остается 50 частей неокисленного ацетилизоэвгенола несмотря на теориетически большое количество окисляющего вещества.
Метод получения 3:
Источник информации: Патент Германии DE475,918 (от 06.05.1929)10,8 г трихлорметилгваяцилкарбинола растворили в 1600 г воды, затем добавили 16,2 г ацетата меди. Быстро происходит обесцвечивание из-за образования соли меди. После продолжительного кипячения в течение нескольких часов, до тех пор, пока извлекаемая проба больше не дает кристаллизации с соляной кислотой ванилин был извлечен из раствора.
Выход 5,5 г ванилина.
Метод получения 4:
Источник информации: Патент Германии DE598,652 (от 14.06.1934)К раствору 69 весовых частей натрия в 2400 весовых частях метанола добавили раствор 271,5 частей 3-метокси-4-оксифенилтрихлорметилкарбинола в 240 частях метанола. Нагревали раствор 4 часа с обратным холодильником, затем подкисляют серной кислотой, отгоняют метанол с водяным паром и исчерпывающе извлекают раствор хлороформом.
При дистилляции в вакууме получают 91 часть (т.е. 60% теории) ванилина с т.кип. 140-145 С при 6 мм.рт.ст.
Метод получения 5:
Источник информации: Патент Германии DE598,652 (от 14.06.1934)Раствор 270 весовых частей гидроксида калия в 480 весовых частях метанола перемешивают при температуре около 20 С с раствором 275,5 частей 3-метокси-4-оксифенилтрихлорметилкарбинола в 480 весовых частях метанола. Реакция протекает при стимулировании ее кипячением. После ее завершения осуществляют еще 0,5 часа нагревания с обратным холодильником. Подкисляют серной кислотой, отгоняют метанол с водяным паром и исчерпывающе извлекают раствор хлороформом.
Было получено 101 часть (66% теории) ванилина.
Способы получения:
- Реакцией 2-метоксифенола с хлороформом и спиртовым раствором щелочи (в водной щелочи выход всего 5%). (выход 99%) [Лит.]
- Реакцией 2-метоксифенола с метилформанилидом в присутствии хлорокиси фосфора. [Лит.]
- Окислением лигнина нитробензолом. [Лит.]
Используется для синтеза веществ:
2-метокси-4-(2-нитропроп-1-енил)фенол
3,4-диметоксибензальдегид
4-метил-2-метоксифенол
Реакции вещества:
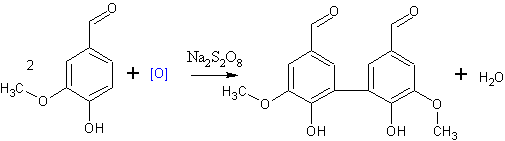
- Окисляется персульфатами в присутствии солей железа(II) до димерного продукта. (выход 100%) [Лит.]
- Реагирует с хлоридом тетраметиламмония в 1,2-диметоксиэтане в присутствии карбоната калия при 145 С при микроволновом облучении в течение 25 минут с образованием 3,4-диметоксибензальдегида. (выход 60%) [Лит.]
- Реагирует с уксусным ангидридом в присутствии ацетата натрия в пиридине с образованием 4-ацетокси-3-метоксикоричной кислоты. (выход 64%) [Лит.]
- Реагирует с малоновой кислотой в присутствии аммиака с образованием 4-гидрокси-3-метоксикоричной кислоты. (выход 50%) [Лит.]
- Реагирует с малоновой кислотой в присутствии пиперидина при нагревании в пиридине с образованием 4-гидрокси-3-метоксикоричной кислоты. (выход 80%) [Лит.]
- С перекисью водорода и гидроксидом натрия образует метоксигидрохинон. (выход 100%) [Лит.]
- Реагирует с уксусным ангидридом в присутствии ацетата натрия с образованием 4-ацетокси-3-метоксикоричной кислоты. [Лит.]
- При кипячении в течение 10 часов со свежеосажденным оксидом ртути(II) в щелочном растворе образует 5-(гидроксимеркур)ванилин. [Лит.]
- Деметилируется под действием хлорида алюминия и пиридина в дихлорметане в течение 24 часов до 3,4-дигидроксибензальдегида. (выход 87%) [Лит.]
- Реагирует с гидрохлоридом гидроксиламина в уксусной кислоте в присутствии ацетата натрия с образованием 4-гидрокси-3-метоксибензонитрила. (выход 80%) [Лит.]
- Восстанавливается амальгамированным цинком при кипячении с концентрированной соляной кислотой и этанолом до 4-метил-2-метоксифенола. (выход 60%) [Лит.]
- Реагирует с N-метилформамидом при 160-175 С в течение 2,5-3 часов с образованием N-(4-гидрокси-3-метоксибензил)метиламина. (выход 92%) [Лит.]
- Феруловая кислота может быть получена реакцией ванилина с малоновой кислотой в присутствии пиперидина в пиридине при комнатной температуре в течение 3 недель. Выход 70-85%. Название реакции: реакция Перкина. [Лит.1
 ]
]
CH3O(HO)C6H3CHO + CH2(COOH)2 → CH3O(HO)C6H3CH=CHCOOH + CO2 + H2O
- 4-Гидрокси-3-метоксибензальдегид реагирует с азотистоводородной кислотой в серной кислоте с образованием 4-гидрокси-3-метоксибензонитрила. Выход 70%. [Лит.1]
Реакции, в которых вещество не участвует:
- Не вступает в реакцию Канниццаро. [Лит.]
Давление паров (в мм рт.ст.):
15 (170°C)
Показатели диссоциации:
pKa (1) = 7,4 (25°C, вода)
Температура вспышки в воздухе (°C):
162Температура самовоспламенения на воздухе (°C):
366Летальная доза (ЛД50, в мг/кг):
2000 (крысы, перорально)
Применение:
Ароматизатор в пищевой промышленности, душистое вещество в парфюмерии. Для придания блеска покрытиям в гальванотехнике. Для синтеза некоторых лекарств.
Дополнительная информация::
Устойчив к окислению, не вступает в реакцию Канниццаро.
Источники информации:
- CRC Handbook of Chemistry and Physics. - 90ed. - CRC Press, 2010. - С. 3-292, 8-106
- Schlager N., Weisblatt J., Newton D.E. Chemical Compounds. - 2006. - С. 873-877
- Seidell A. Solubilities of organic compounds. - 3ed., vol.2. - New York: D. Van Nostrand Company, 1941. - С. 589-590
- Yalkowsky S.H., Yan H. Handbook of aqueous solubility data. - CRC Press, 2003. - С. 479
- Брюсова Л.Я. Химия и технология синтетических душистых веществ. - М.: Пищепромиздат, 1947. - С. 372-398
- Войткевич С.А. 865 душистых веществ для парфюмерии и бытовой химии. - М.: Пищевая промышленность, 1994. - С. 411-412
- Исагулянц В. Синтетические душистые вещества. - Ереван: Издательство академии наук Армянской ССР, 1946. - С. 345-356
- Основы органической химии душистых веществ для прикладной эстетики и ароматерапии. - М.: ИЦ Академкнига. - 2006. - С. 183-186
- Петрова Л.Н., Шварц О.В. Анализ синтетических душистых веществ. - М.-Л.: Пищепромиздат, 1941. - С. 145
- Препаративная органическая химия. - М., 1959. - С. 326
- Справочник химика. - Т. 2. - Л.-М.: Химия, 1964. - С. 570-571
- Хейфиц Л.А., Дашунин В.М. Душистые вещества и другие продукты для парфюмерии. - М.: Химия, 1994. - С. 155-157
- Химическая энциклопедия. - Т. 1. - М.: Советская энциклопедия, 1988. - С. 352-353
- Химический энциклопедический словарь. - Под ред. Кнунянц И.Л. - М.: Советская энциклопедия, 1983. - С. 94
Если не нашли нужное вещество или свойства можно выполнить следующие действия:
Если вы нашли ошибку на странице, выделите ее и нажмите Ctrl + Enter.
© Сбор и оформление информации: Руслан Анатольевич Кипер